"Dentro la macchina: come le sostanze psichedeliche riscrivono il cervello"
Dal recettore 5-HT2A alla Default Mode Network, dal blocco NMDA alla ketamina come antidepressivo: una mappa dei meccanismi d'azione — e di cosa ci dicono sulla natura ordinaria della coscienza. Serie: Psicotropi, mente e biologia·2
Neuroscienze - Psichedelici 2
Dal recettore 5-HT2A alla Default Mode Network, dal blocco NMDA alla ketamina come antidepressivo: una mappa dei meccanismi d'azione — e di cosa ci dicono sulla natura ordinaria della coscienza.
Serie: Psicotropi, mente e biologia·
Nel primo episodio abbiamo visto come la classificazione delle sostanze psichedeliche sia un atto politico, non farmacologico. Ora entriamo nella biologia. Perché capire il meccanismo d'azione di queste molecole non è solo un esercizio accademico: è l'unico modo per valutare razionalmente rischi, potenziale terapeutico e — per chi si occupa di ottimizzazione cognitiva — quello che queste sostanze ci dicono sul funzionamento ordinario del cervello.
La domanda di partenza sembra semplice: come fa una molecola ingerita o inalata a produrre un'alterazione così radicale dell'esperienza soggettiva? La risposta coinvolge recettori specifici, reti cerebrali, neurotrasmettitori — e, nel caso della ketamina, un meccanismo talmente inaspettato da aver costretto la psichiatria a riconsiderare vent'anni di assunzioni sulla depressione.
I — Il recettore chiave
Il 5-HT2A: il portale della maggior parte degli psichedelici classici
LSD, psilocina (la forma attiva della psilocibina dopo la digestione), DMT, mescalina, 2C-B. Molecole chimicamente diverse, effetti soggettivamente diversi — eppure condividono un bersaglio molecolare comune: il recettore della serotonina 5-HT2A (5-idrossitriptamina, sottotipo 2A).
Per capire cosa succede quando questo recettore viene attivato da uno psichedelico, bisogna prima capire cosa fa normalmente. Il 5-HT2A è distribuito in modo non uniforme: si concentra soprattutto nella corteccia prefrontale, nel talamo e nelle aree visive associative. La serotonina endogena lo attiva in modo fisiologico, modulando l'eccitabilità neuronale in tono basso e ritmato. Gli psichedelici lo attivano in modo sostenuto e molto più potente — con un'affinità, nel caso dell'LSD, straordinariamente alta e con cinetica di dissociazione lentissima (rimane "agganciato" al recettore per ore).
Glossario — recettori e agonismo
Recettore Proteina sulla superficie (o all'interno) di una cellula neuronale che riconosce e lega molecole specifiche — neurotrasmettitori endogeni o sostanze esterne. Quando il legame avviene, cambia l'attività della cellula.
Agonista Una sostanza che si lega a un recettore e lo attiva, mimando o amplificando l'effetto del ligando naturale. LSD e psilocina sono agonisti del 5-HT2A: occupano il sito della serotonina e lo attivano più a lungo e più intensamente di quanto farebbe la serotonina stessa.
Il risultato di questa attivazione sostenuta è una cascata di effetti che si propagano dall'interno della cellula (tramite proteine G e secondi messaggeri) fino all'attività di reti cerebrali intere. Ma il luogo dove questo processo diventa fenomenologicamente rilevante è il talamo.
II — Il filtro che crolla
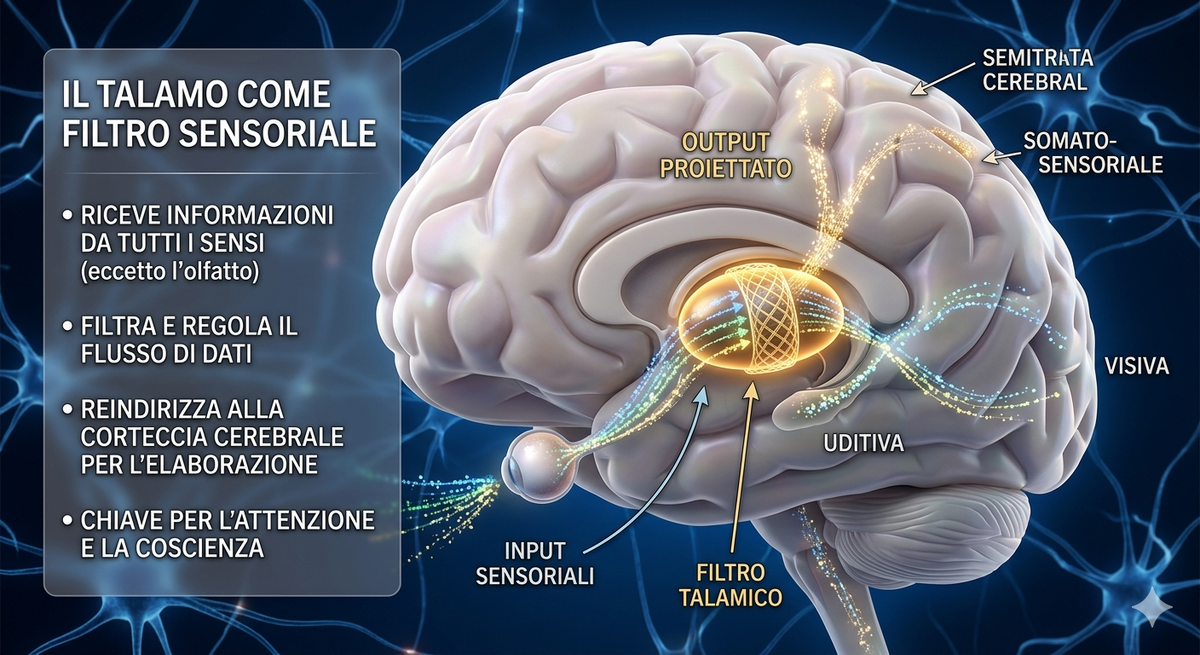
Il talamo come guardiano della coscienza
Il talamo è una struttura profonda, grossomodo a forma di uovo, posizionata al centro del cervello. Il suo ruolo è spesso descritto con una metafora: è il centralino — o più precisamente, il filtro. Ogni secondo, il cervello riceve un flusso enorme di segnali sensoriali (visivi, uditivi, propriocettivi, interocettivi). Il talamo decide quali di questi segnali vengono inoltrati alla corteccia e quali vengono soppressi o attenuati.
Questo filtraggio è adattivo: ci permette di concentrarci su ciò che è rilevante e ignorare il rumore di fondo. È la base neurologica dell'attenzione selettiva. Senza di esso, ogni stimolo avrebbe lo stesso peso — un'esperienza potenzialmente caotica.
Schema — il talamo come filtro: stato ordinario vs stato psichedelicoStato ordinarioInput sensorialesegnali grezzi↓Talamofiltra, seleziona, sopprime↓Cortecciariceve segnale selezionatopercezione ordinaria, stabileSotto psichedelici (5-HT2A)Input sensorialesegnali grezzi↓Talamofiltro compromesso, 5-HT2A attivo↓Cortecciainondazione di segnali non filtratiallucinazioni, sinestesie, distorsioni
L'attivazione sostenuta del 5-HT2A nel talamo — e nei neuroni piramidali della corteccia che ricevono i suoi output — altera questo filtraggio. La soppressione si riduce. Segnali che normalmente non raggiungono la coscienza iniziano a emergere. La corteccia visiva riceve input spontanei che interpreta come percezioni reali: da qui le allucinazioni geometriche, le sinestesie (sentire i colori, vedere i suoni), le distorsioni della forma e del tempo.
Ma la vera storia non riguarda solo le percezioni. Riguarda la rete cerebrale che gestisce il senso del sé.
III — La rete che credi di essere
La Default Mode Network e la dissoluzione dell'ego
Negli anni 2000, gli studi di neuroimaging a riposo (fMRI con soggetti fermi e non impegnati in compiti specifici) hanno identificato una rete di regioni cerebrali che si attiva in modo coordinato quando il cervello è "a riposo" — ma che si disattiva durante compiti che richiedono attenzione esterna. L'hanno chiamata Default Mode Network (DMN), rete in modalità predefinita.
Le aree principali della DMN includono la corteccia prefrontale mediale, la corteccia cingolata posteriore, il precuneo e la giunzione temporo-parietale. Funzionalmente, la DMN è associata a: pensiero autobiografico (ricordi, proiezioni future), elaborazione del senso del sé, ruminazione, giudizio sociale, narrazione interna. In sintesi: è la rete che produce la storia che racconti di te stesso.
"La DMN è la struttura neurale dell'ego — e gli psichedelici la spengono."
Robin Carhart-Harris, Imperial College London, 2014
Gli studi di Robin Carhart-Harris e colleghi all'Imperial College — tra i primi a usare fMRI con psilocibina in soggetti umani — hanno mostrato che gli psichedelici riducono drasticamente la coerenza interna della DMN. Le aree che normalmente si attivano e disattivano in sincronia perdono la loro coordinazione. Le connessioni funzionali si indeboliscono.
La corrispondenza soggettiva di questo fenomeno è quello che la letteratura psichedelica chiama ego dissolution: la perdita del confine tra sé e ambiente. In forma lieve, si manifesta come senso di unità con il contesto, riduzione della ruminazione, apertura emotiva insolita. In forma intensa (dosi alte), può produrre la completa dissoluzione del senso di essere un soggetto separato — un'esperienza descritta come mistica, terrificante o entrambe le cose.
Glossario — ego dissolution e oceanic boundlessness
Ego dissolution Termine tecnico usato in neuroscienze e psicofarmacologia per descrivere la riduzione o scomparsa temporanea del senso ordinario del sé come entità separata. Misurata con scale validate (MEQ30, EDI). Non equivale a perdita di coscienza: il soggetto rimane sveglio e reattivo, ma il "chi sta vivendo l'esperienza" diventa sfocato o assente.
Oceanic boundlessness Uno dei tre fattori principali della scala 5D-ASC (Altered States of Consciousness) — il senso di espansione, fusione con l'ambiente, trascendenza del tempo. Correlato positivamente con gli outcomes terapeutici negli studi su depressione e fine vita.
L'implicazione terapeutica è significativa. In soggetti con depressione maggiore o PTSD, la DMN è spesso iperattiva e rigida: il pensiero autobiografico si inceppa in loop ruminativi, il senso del sé diventa una prigione narrativa. Ridurne temporaneamente la dominanza sembra offrire una finestra di plasticità — un momento in cui i pattern cognitivi possono essere rimessi in discussione. Non è magia: è neuroplasticità indotta farmacologicamente.
IV — Un sistema completamente diverso
Il glutammato, l'NMDA e perché la ketamina funziona in sei ore
Fino a qui abbiamo parlato di serotonina. Ora cambiamo sistema — e il cambio è radicale. I dissociativi (ketamina, PCP, metossicetamina) non toccano il 5-HT2A. Agiscono sul recettore NMDA del glutammato.
Il glutammato è il principale neurotrasmettitore eccitatorio del cervello — opposto e complementare al GABA, che è il principale inibitore. Il recettore NMDA (N-metil-D-aspartato) è un canale ionico: quando si apre, lascia entrare calcio e sodio nella cellula, amplificando il segnale eccitatorio. È fondamentale per la plasticità sinaptica, la memoria a lungo termine e l'apprendimento associativo.
Glossario — glutammato e canale NMDA Recettore NMDA Canale ionico ligando-dipendente che si apre quando si legano contemporaneamente glutammato e glicina — e richiede anche la depolarizzazione della membrana (per rimuovere il blocco da ioni magnesio). È un "sensore di coincidenza": si attiva solo quando la cellula è già parzialmente eccitata. Ketamina e PCP lo bloccano dall'interno del canale (blocco open-channel), impedendo il flusso di ioni anche quando il recettore è attivato.
La ketamina blocca il recettore NMDA dall'interno del canale. Quando il canale si apre, la ketamina entra e lo tappa — impedendo il flusso ionico. Questo produce effetti diversi a seconda della dose: a dosi subanestetiche (le dosi usate in clinica), produce analgesia, dissociazione lieve, e — la scoperta più sorprendente degli ultimi vent'anni — un effetto antidepressivo rapidissimo.
Il perché di questo effetto è ancora oggetto di ricerca attiva, ma il modello più accreditato funziona così: il blocco NMDA in certi circuiti (in particolare nei neuroni GABAergici inibitori) produce un rimbalzo eccitatorio — un aumento paradossale di glutammato disponibile in altre sinapsi. Questo stimola recettori AMPA, che a loro volta attivano la produzione di BDNF (Brain-Derived Neurotrophic Factor), una proteina che favorisce la crescita e il rimodellamento delle sinapsi. Il risultato è un rapido ripristino delle connessioni sinaptiche nelle aree prefrontali — le stesse che si "assottigliano" nella depressione cronica.
Schema — meccanismo antidepressivo della ketamina Ketamina blocca NMDA→Neuroni GABAergici inibizione ridotta→Rimbalzo glutammato attivazione AMPA↓Produzione BDNF fattore neurotrofico→Rimodellamento sinaptico corteccia prefrontale effetto antidepressivo in 2–6 ore (vs 4–6 settimane degli SSRI)
Questo meccanismo spiega perché la ketamina funziona in ore, mentre gli SSRI richiedono settimane. Gli SSRI agiscono sulla disponibilità di serotonina — un processo che produce neuroadattamenti lenti. La ketamina rimodella fisicamente le sinapsi. Non è la stessa classe di intervento: è una differenza qualitativa, non quantitativa.
La FDA ha approvato l'esketamina (Spravato, isomero S della ketamina) per la depressione resistente nel 2019 e per il rischio suicidario acuto nel 2020. È la prima molecola con meccanismo non-monoaminergico approvata per la depressione in settant'anni. La cosa imbarazzante, per il sistema regolatorio, è che questo è avvenuto solo perché la ketamina era già un anestetico approvato — e quindi non soggetta alle restrizioni dello Schedule I. Un incidente burocratico che ha salvato vite.
V — Il caso anomalo
Salvinorina A: quando la serotonina non c'entra nulla
La Salvia divinorum è una pianta della famiglia della menta, usata da secoli nelle cerimonie dei Mazatec in Oaxaca, Messico. Il suo principio attivo, la salvinorina A, è l'unico psichedelico potente conosciuto che non agisce né sulla serotonina né sul glutammato. È un agonista selettivo dei recettori κ-oppioidi (KOR — kappa opioid receptor).
I recettori κ-oppioidi si trovano in strutture come il nucleo accumbens, l'amigdala e la corteccia cingolata anteriore — aree centrali nell'elaborazione del dolore, della ricompensa, della memoria emotiva. La loro attivazione produce effetti radicalmente diversi dagli psichedelici serotoninergici: non allucinazioni visive elaborate ma una dissociazione profonda, corporea, spesso descritta come spaesante e difficile da integrare. L'effetto è brevissimo (10–20 minuti se inalata) ma di grande intensità.
Approfondimento — recettori oppioidi: non tutti uguali
I tre recettori oppioidi principali Il sistema oppioide endogeno ha tre recettori principali: μ (mu), δ (delta) e κ (kappa). I recettori μ sono quelli attivati da morfina, eroina, ossicodone — responsabili dell'analgesia intensa, dell'euforia e della dipendenza. I recettori κ producono effetti opposti: analgesia, ma anche disforia, percezioni dissociative e alterazioni della coscienza senza euforia. La salvinorina A è un agonista κ di potenza straordinaria — ed è la prima sostanza psicotropa naturale non alcaloide mai identificata.
Il significato scientifico della salvinorina A va oltre la sua singolarità farmacologica: dimostra che esistono almeno due "portali" neurali verso stati alterati profondi — il sistema serotoninergico e il sistema κ-oppioide — con fenomenologie soggettive molto diverse. Questo suggerisce che l'alterazione della coscienza non sia un fenomeno unitario con un unico substrato, ma un territorio con meccanismi multipli, ancora in gran parte inesplorati.
VI — Confronto sinottico
Quattro classi, quattro meccanismi
Psichedelici classici MolecoleLSD, psilocina, DMT, mescalinaTargetRecettore 5-HT2A Sistema Serotoninergico Dipendenza fisica Assente Durata 4–12 ore
Dissociativi Molecole Ketamina, PCP, MXE Target Recettore NMDA Sistema Glutamatergico Dipendenza fisica Possibile (ketamina) Durata 45 min – 2 ore
Entactogeni Molecole MDMA, MDA Target SERT, NET, DAT Sistema Monoaminergico Dipendenza fisica Bassa Durata3–5 ore Kappa-oppioidi Molecole
Salvinorina A TargetRecettore κ-oppioide Sistema Oppioide (KOR) Dipendenza fisica Non documentata Durata 10–30 minuti
VII — La variabile che la chimica non spiega
Set, setting e il limite del modello molecolare
Nessuna descrizione farmacologica è sufficiente. Questo non è misticismo — è empirismo. La stessa molecola, alla stessa dose, nello stesso soggetto, produce esperienze radicalmente diverse a seconda del set (stato mentale, aspettative, storia psicologica) e del setting (ambiente fisico, presenza o assenza di altre persone, contesto culturale).
Gli studi della Johns Hopkins hanno sistematizzato questo dato in modo rigoroso. I partecipanti preparati con sessioni psicoterapeutiche preliminari, supportati durante l'esperienza da guide formate e integrati con sessioni successive mostrano outcomes profondamente diversi da quelli esposti alla stessa sostanza in contesti non strutturati. La differenza non è marginale: è la differenza tra un'esperienza terapeuticamente significativa e un episodio acuto di panico o psicosi reattiva.
Per chi ragiona in termini di biohacking, questa è una variabile di sistema — non un dettaglio. Ottimizzare una molecola ignorando il contesto d'uso è come ottimizzare un protocollo di allenamento ignorando il sonno e la nutrizione. Il substrato biologico è necessario ma non sufficiente.
Sintesi dell'episodio — meccanismi principali
5-HT2A (psichedelici classici): attivazione del recettore serotoninergico → alterazione del filtro talamico → inondazione corticale → dissoluzione della DMN → ego dissolution.
NMDA (dissociativi): blocco open-channel del recettore glutamatergico → dissociazione senso-motoria → rimbalzo AMPA → BDNF → rimodellamento sinaptico → effetto antidepressivo rapido.
Monoamine (entactogeni): rilascio massiccio di serotonina, dopamina e noradrenalina → empatia, riduzione paura, apertura emotiva. In studio per PTSD.
κ-oppioidi (salvinorina A): agonismo KOR → dissociazione corporea profonda senza componente serotoninergica. Dimostra l'esistenza di un secondo portale verso stati alterati.
Nel prossimo episodio: il potenziale terapeutico — dove la ricerca è arrivata davvero. Depressione resistente, PTSD, disturbi da uso di sostanze, fine vita. Cosa dicono gli studi di fase II e III, cosa il sistema regolatorio europeo non sa ancora come gestire.
Fonti principali
Carhart-Harris R. et al., "Neural correlates of the psychedelic state as determined by fMRI studies with psilocybin", PNAS (2012). — Vollenweider F.X. & Preller K.H., "Psychedelic drugs: neurobiology and potential for treatment of psychiatric disorders", Nature Reviews Neuroscience (2020). — Zanos P. & Gould T.D., "Mechanisms of ketamine action as an antidepressant", Molecular Psychiatry (2018). — Roth B.L. et al., "Salvinorin A: a potent naturally occurring nonnitrogenous κ opioid selective agonist", PNAS (2002). — Nichols D.E., "Psychedelics", Pharmacological Reviews (2016).
Questo articolo ha scopo divulgativo e scientifico. Non costituisce guida all'uso di sostanze controllate.